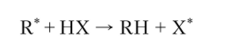Как уже отмечалось, полимерные материалы в процессе эксплуатации обычно подвергаются одновременному воздействию различных факторов, инициирующих деструкцию. Наиболее часто встречающаяся термоокислительная деструкция протекает по ценному механизму с вырожденным разветвлением. Она также включает стадии инициирования (образование полимерных гидроперекисей и их распад), развития и обрыва цени. Рассмотрим этот процесс на примере термоокислительной деструкции полипропилена.
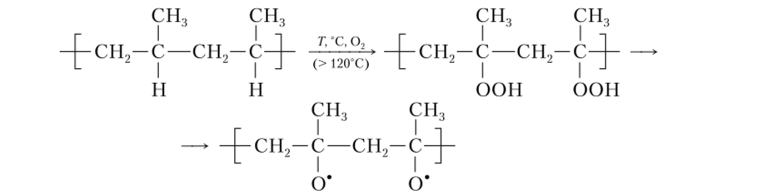
1. Инициирование'.
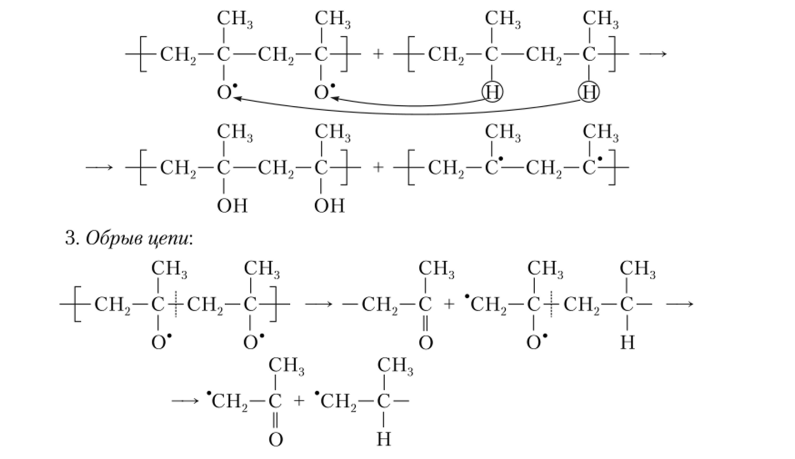
2. Развитие цепи. Распад гидроперекисей, сопровождающийся образованием активных радикалов, инициирует новые реакционные цепи, так что процесс окисления постепенно ускоряется:
Главная причина старения полимеров — окисление их молекулярным кислородом, протекающее особенно быстро при повышенных температурах; часто инициируется светом, остатками инициаторов, примесями металлов переменной валентности. С целью повышения устойчивости полимера или полимерного материала к действию различных факторов в условиях переработки, хранения и эксплуатации применяют совокупность методов, направленных на стабилизацию полимеров. Основной способ стабилизации полимеров с целью предупреждения нежелательных процессов деструкции — это введение в полимер специальных добавок, называемых стабилизаторами. Роль стабилизаторов сводится либо к предотвращению образования свободных радикалов, либо к взаимодействию молекул стабилизатора (ИХ) с радикалами роста и переводу их в неактивную форму, например, по реакции.
Результатом деструкции является появление межмакромолекулярных сшивок и различных продуктов окисления:
где X* — неактивный радикал. В качестве стабилизаторов (антиоксидантов) используют органические соединения, содержащие подвижные атомы водорода: вторичные ароматические амины и замещенные фенолы.
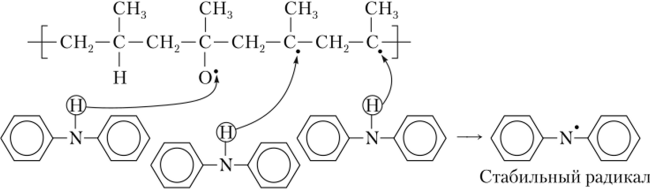
Механизм стабилизации полимеров при термоокислителыюй деструкции предполагает захват активного радикала молекулой стабилизатора (антиоксиданта). При этом образуется малоактивный радикал:
Введение
в полимер стабилизатора увеличивает период индукции (т), определяющий время работоспособности антиоксиданта (рис. 6.2).

Рис. 6.2. Кинетические кривые окисления полипропилена в присутствии антиоксиданта:
р|0,] — давление кислорода в процессе окисления; С, < С2 < С, — концентрация стабилизатора Кроме стабилизаторов широко применяют также антиоксиданты — вещества, способные разрушать гидропероксиды, сульфиды, сульфоксиды, фосфиты или металлы, оксиды переходных металлов в низшей валентной форме, например, по реакции.